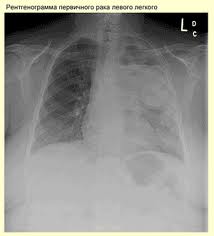
Причина заболевания
Ни одно из широко рапространенных онкологических заболеваний не имеет столь очевидной связи с факторами окружающей среды, условиями производства, вредными привычками и индивидуальным стилем жизни, как рак легкого. Рост заболеваемости отражает нарастание вредного воздействия современной индустрии на организм человека, что особенно заметно в странах Европы и Северной Америки.
Канцерогенное действие на легочную ткань оказывают многие химические вещества: полициклические ароматические углеводороды, входящие в состав продуктов термической обработки угля и нефти (смолы, коксы, газы и др.), ряд простых органических веществ (хлорметиловые эфиры, винилхлорид и др.), некоторые металлы и их соединения (мышьяк, хром, кадмий).
Существенное загрязнение окружающей воздушной среды канцерогенами вызывают двигатели внутреннего сгорания и промышленные выбросы в атмосферу. Особенно много бензпирена образуется при форсированной работе двигателей, при разгоне и торможении автотранспорта, при взлете и посадке реактивных лайнеров. Следует упомянуть о производственных вредностях. Еще в начале XX века было установлено, что высокая заболеваемость раком легкого у шахтеров Саксонии связана с высоким содержанием радиоактивных примесей в руде. Влияние ионизирующей радиации доказано при обследовании шахтеров урановых рудников в США.
Повышена заболеваемость раком легкого у рабочих сталелитейной, деревообрабатывающей, металлургической промышленности, керамического асбестно-цементного и фосфатного производства; у лиц, контактирующих с соединениями хрома, подвергающихся воздействию каменной пыли, занятых в никелевой и алюминиевой промышленности, у шоферов. Между тем промышленное загрязнение и профессиональные вредности не играли бы столь большой роли в росте заболеваемости, если бы не сочетались с крайне вредной привычкой — курением. Курящие шахтеры в урановых рудниках, как и курящие рабочие асбестовой промышленности, заболевают раком легкого гораздо чаще, чем некурящие. Увеличение заболеваемости раком легкого во всех странах находится в прямой зависимости от роста потребления сигарет и числа курящих. У курящих более двух пачек в сутки риск возникновения рака этой локализации в 25 раз выше. Рост заболеваемости среди женщин также связывают с распространением привычки женщин курить, однако нельзя исключить влияние возросшего потребления гормональных препаратов. Совокупные неблагоприятные воздействия вызывают фоновые предраковые изменения слизистой бронхов, играющие важную роль в патогенезе центрального рака легкого. Не вызывает сомнений факт значительной частоты возникновения рака легкого из рубца у лиц с воспалительными заболеваниями легких в анамнезе.
Основными факторами риска развития рака легкого являются:
1. Генетические факторы.
• Первичная множественность опухолей (излеченный пациент от злокачественной опухоли).
• Три случая развития рака легкого в семье (у ближайших родственников)и более.
2. Модифицирующие факторы.
• Экзогенные:
— курение;
— загрязнение окружающей среды канцерогенами;
— профессиональные вредности.
• Эндогенные:
— возраст более 50 лет;
— хронические легочные заболевания (туберкулез, пневмония, бронхит, локализованный пневмофиброз и др.);
— эндокринные заболевания.
Перечисленные факторы определяют одно из главенствующих направлений в борьбе с этим недугом — профилактику рака легкого. Согласно терминологии ВОЗ профилактические мероприятия предусматривают первичную и вторичную профилактику.
Первичной (онкогигиенической, иммунобиологической, законодательно-правовой) профилактикой является система государственных и медицинских мероприятий, направленных на устранение или резкое уменьшение воздействия на организм веществ и факторов, признаваемых в настоящее время канцерогенными и играющими значительную роль в возникновении и развитии злокачественного процесса. Основной целью гигиенической профилактики рака легкого является борьба с загрязнением вдыхаемого воздуха или хотя бы за уменьшение степени его загрязнения, с производственными (профессиональными) вредностями и крайне вредной привычкой— курением табака.
Вторичная или клиническая (медицинская) профилактика предусматривает планово-организационную систему обследования (диспансеризации) населения с целью выявления, учета и лечения фоновых процессов и предопухолевых заболеваний легких — факторов повышенного риска рака легкого. К категории «повышенного риска» относятся пациенты, болеющие хроническим бронхитом, пневмонией или туберкулезом, длительно курящие мужчины в возрасте 50 лет и старше, а также излеченные от злокачественного заболевания. Диспансерное наблюдение с периодическим обследованием этого контингента больных направлено одновременно на выявление истинно ранних форм рака легкого, лечение которых дает хорошие отдаленные результаты.
Симптомы рака
Клиническая симптоматика зависит от клинико-анатомической формы и гистологической структуры, локализации, размеров и типа роста опухоли, характера метастазирования, сопутствующих воспалительных изменений в бронхах и легочной ткани.
При центральном раке легкого группы клинических симптомов по патогенетическому механизму подразделяют на: 1) первичные, или местные, симптомы, обусловленные появлением в просвете бронха первичного опухолевого узла (кашель, кровохарканье, одышка и боли в грудной клетке); эти симптомы, как правило, ранние; 2) вторичные симптомы, которые развиваются в результате сопутствующих бронхогенному раку осложнений воспалительной природы либо обусловлены регионарным или отдаленным метастазированием, вовлечением соседних органов (эти симптомы обычно более поздние и появляются при относительно распространенном опухолевом процессе); 3) общие симптомы (слабость, утомляемость, похудание, снижение трудоспособности и др.), являющиеся следствием общего воздействия на организм развивающейся опухоли и сопутствующих воспалительных осложнений.
Характер симптомов, время их проявления и степень выраженности определяются исходной локализацией опухоли в одном из бронхов, формой ее роста (эндо- или перибронхиального) и распространенностью процесса. Чем крупнее пораженный бронх, особенно при экзофит-ном (эндобронхиальном) росте опухоли, тем ярче начальные симптомы заболевания и тяжелее клиническая картина осложнений, обусловленных стенозом бронха(ов).
Наиболее характерной чертой в клинической картине центрального рака легкого являются признаки обтурационного пневмонита (повышение температуры), который имеет ряд типичных черт: быстротечность, рецидивирование, а также развитие на фоне сегментарного или долевого ателектаза со специфической рентгенологической семиотикой. У мужчин старше 50 лет, особенно курящих, появление рецидивирующего пневмонита позволяет предположить рак легкого.
Объективное обследование (наружный осмотр, перкуссия, аускультация) имеет при раке легкого второстепенное значение, особенно при его распознавании на ранних этапах заболевания. В поздней стадии клиническая картина центрального рака осложняется симптомами его распространения за пределы пораженного легкого с вовлечением в процесс плевры, возвратного и диафрагмального нервов, а также метастазами в отдаленных органах. Эти признаки, естественно, имеют не столько диагностическое, сколько прогностическое значение. В таких случаях методы физикального исследования могут сыграть ведущую роль, заменив более сложные методики.
Периферический рак легкого долгое время протекает без клинических симптомов и, как правило, распознается довольно поздно. Первые симптомы выявляются лишь тогда, когда опухоль начинает оказывать давление на рядом расположенные структуры и органы или прорастает их. Наиболее характерными симптомами периферического рака легкого являются боли в грудной клетке и одышка.
Прорастание бронха сопровождается кашлем и кровохарканьем, но эти симптомы не являются ранними, как при центральном раке. Нередко отмечаются симптомы общего воздействия опухоли на организм больного: слабость, повышение температуры, утомляемость, снижение трудоспособности и др.
В более поздней стадии заболевания, когда опухоль распространяется на крупный бронх и суживает его просвет, клиника периферического рака становится сходной с таковой центрального. На данной стадии заболевания результаты физикального исследования одинаковы при обеих формах рака легкого. Однако, в отличие от центрального рака, при рентгенологическом исследовании на фоне ателектаза выявляется тень самой периферической опухоли. При периферическом раке опухоль нередко распространяется по плевре с образованием плеврального выпота.
«Полостная» форма периферического рака является результатом некроза, расплавления тканей в центре опухоли. Эта форма рака сопровождается признаками воспалительного процесса (кашель, необильное отхож-дение мокроты, кровохарканье, повышение температуры). Деструкция в опухоли чаще наблюдается у лиц мужского пола, в возрасте старше 50 лет и при больших размерах опухолевого узла.
Рак верхушки легкого представляет собой разновидность периферического рака. Его клиническая симптоматика является результатом прорастания опухоли через купол плевры плечевого сплетения, поперечных отростков и дужек нижних шейных позвонков, а также симпатического нерва (боли в плечевом суставе и плече). Прогрессирует атрофия мышц дистальных отделов предплечья и развивается синдром Бернара— Горнера (миоз, птоз, энофтальм). Данный симптомоком-плекс, описанный Pancoast в 1924 г., может наблюдаться при различных опухолевых процессах, локализующихся в верхней апертуре грудной клетки (по словам самого автора, при опухолях верхней легочной борозды).
Атипичные клинико-анатомические формы рака легкого встречаются реже. Медиастинальная форма рака легкого проявляется множественными метастазами в лимфатических узлах средостения, при этом первичную опухоль в легком всеми доступными клиническими методами выявить не удается. Рентгенологически она симулирует опухоль средостения с клиническими признаками сдавления его органов и сосудов (синдром сдавления верхней полой вены (отечность лица и шеи, расширение вен передней грудной стенки и шеи, цианоз), охриплость, афония, поперхивание жидкой пищей и др.). Карциноматоз характеризуется множественными узлами в легких, когда первичный узел рака не известен. Клинически он проявляется одышкой и общими симптомами, а рентгенологически напоминает милиарный туберкулез легких и другие диссеминиро-ванные заболевания.
При раке легкого выделяют группу паранеоплас-тических синдромов, связанных с гиперпродукцией гормонов (синдром секреции адренокортикотропного, антидиуретического, паратиреоидного гормонов, эстрогенов, серотонина). Эти синдромы в большей степени характерны для мелкоклеточного рака. Рак легкого может сопровождаться тромбофлебитом, различными вариантами нейро- и миопатии, своеобразными дерматозами, нарушениями жиролипидного обмена.
Гормоноподобные субстанции — своеобразные маркеры малигнизации; их можно обнаружить радиоиммунологическими методами. Чаще всего наблюдается секреция опухолью АКТГ или его метаболических предшественников. Уровень кортикостероидов в сыворотке крови и моче таких больных нередко выше, чем при синдроме Кушинга, и его труднее блокировать медикаментозное Клинически у 3—5% больных раком легкого выявляются артралгический и ревматоидный синдромы, легочная остеоартропатия, гинекомастия, невриты, дерматомиозиты, сосудистые тромбозы. Подобные проявления часто исчезают после излечения больного.
Рак легкого первоночально часто может проявляться своеобразным синдромом — гипертрофической легочной остеоартропатией Мари—Бамбергера, заключающейся в утолщении и склерозе длинных трубчатых костей голеней и предплечий, мелких трубчатых костей кистей и стоп, припухлости суставов (локтевых, голеностопных), колбовидном утолщении концевых фаланг пальцев кистей («барабанные палочки»).
Диагностика
При установлении диагноза рака легкого решающая роль принадлежит специальным методам исследования. В зависимости от клинико-анатомической формы рака обязательные и дополнительные методы исследования должны быть применены в определенной последовательности.
Обязательные методы исследования (первичная диагностика):
1. Общеклиническое обследование.
2. Рентгенологическое исследование органов грудной клетки:
рентгенографию в двух проекциях (прямой и боковой);
• контрастное исследование пищевода для оценки состояния бифуркационных лимфатических узлов;
• томо(зоно)графию:
— в прямой проекции в срезе бифуркации трахеи (оценка состояния трахеи, главных и промежуточного бронхов, а также основных групп внут-ригрудных лимфатических узлов);
— в косых проекциях (получение изображения верхнедолевых бронхов и их сегментарных ветвей) — при центральном раке;
— в боковой проекции (получение изображения промежуточного, нижнедолевых и среднедоле-вого бронхов) — при центральном раке;
— прицельную в прямой и (или) боковой проекциях (в срезе патологической тени) — при периферическом раке;
• компьютерную томографию.
3. Цитологическое исследование мокроты (3—5 анализов), особенно после бронхоскопии.
4. Бронхологическое исследование с получением материала для морфологического исследования (отпечатки опухоли, прямая биопсия — при центральном раке; зондирование бронхов под рентгнологическим контролем — при периферическом раке, катетеризационная биопсия, транстрахеобронхиальная пункция лимфатических узлов).
5. Трансторакальную (чрескожную) пункцию опухоли — при периферическом раке.
6. Ультразвуковое исследование брюшной полости, забрюшинного пространства, надключичных зон.
Для уточняющей диагностики нередко необходимо применение по показаниям специальных дополнительных методов исследования.
Лечение
Лечебная тактика при раке легкого не однозначна. Для правильного выбора метода лечения следует знать основные факторы прогноза: стадию заболевания в соответствии с Международной классификацией по системе TNM, гистологическую структуру опухоли и степень анаплазии, характер и тяжесть сопутствующих заболеваний, функциональные показатели жизненно важных органов и систем. Метод лечения сам по себе является одним из решающих прогностических факторов, значение которого тем больше, чем ближе вариант к радикальному. При лечении больных немелкокле-точным раком легкого применяют следующие методы: хирургическое лечение, лучевую терапию, химиотерапию, комбинированное лечение (операция и лучевая или химиотерапия), химио-лучевое лечение.
Хирургическое лечение больных с резектабель-ными формами рака легкого является радикальным, наиболее обнадеживающим методом, дающим реальные перспективы полного излечения. К абсолютным онкологическим противопоказаниям к операции на легком при раке относят: морфологически потверж-денные метастазы в отдаленных органах (исключая надпочечник и головной мозг) и лимфатических узлах; обширное прорастание опухоли или метастазов в аорту, верхнюю полую вену, пищевод и противоположный главный бронх, что не позволяет выполнить их резекцию; метастатическое поражение париетальной плевры со специфическим плевритом. Комбинированная операция с резекцией бифуркации трахеи, предсердия, пищевода, аорты, верхней полой вены нередко позволяет выполнить радикальное оперативное вмешательство.
Среди противопоказаний к оперативному вмешательству наибольшее значение придают функциональной недостаточности жизненно важных органов и систем больного, т.е. «функциональной неоперабельности»: некомпенсированная сердечная недостаточность II и III степени; выраженные органические изменения в сердце; гипертоническая болезнь III ст.; почечная или печеночная недостаточность. Перечисленные противопоказания имеют относительный характер и необоснованный отказ от операции может лишить больного перспектив выздоровления. Современные возможности анестезиологии и интенсивной терапии позволяют предотвратить нарушения функции органов и систем, особенно при адекватной предоперационной подготовке. Отказ от операции с онкологических позиций также должен быть серьезно мотивирован. Этот вопрос неоходимо решать коллегиально с обязательным участием торакального хирурга, имеющего опыт хирургического лечения рака легкого.
Основными условиями радикализма операции являются: удаление единым блоком легкого или доли и всех ипсилатеральных регионарных внутрилегочных и средо-стенных лимфатических узлов с окружающей клетчаткой в пределах здоровых тканей; отстояние линии пересечения бронха на 1,5—2 см от видимого края опухоли; отсутствие опухолевых клеток в краях пересеченных бронха, сосудов и дополнительно резецированных органов и тканей. Выбор объема и характера операции зависит от локализации и распространенности первичной опухоли, ее отношения к окружающим органам и структурам, состояния внутригрудных лимфатических узлов. Основными операциями при раке легкого являются пневмонэктомия и лобзктомия, а также их варианты (расширенная и комбинированная операция, лобзктомия с циркулярной резекцией бронхов и др.). Пятилетняя выживаемость больных после хирургического лечения при IA стадии (T1N0M0) составляет 53—82%, IB стадии (T2N0M0) — 45—69%. Бронхопластические операции расширяют возможности хирургического метода и способствуют повышению резектабельности, составляющей до 20% среди впервые выявленных больных раком этой локализации. В последние годы с успехом применяют альтернативные методы эндоскопического лечения carcinoma in situ и микроинвазивного рака: лазерная деструкция, электроэксцизия опухоли, фотодинамическая терапия, иногда в сочетании с лучевой терапией.
При периферическом раке легкого и размерах опухоли до 3 см у высокоселективной группы больных (низкие функциональные резервы и т.д.) допустима классическая сегментэктомия с раздельной обработкой элементов корня сегмента, обязательным удалением бронхопульмональных, корневых и средостенных лимфатических узлов.
При II стадии немелкоклеточного рака легкого, т.е. при распространении опухоли на главный бронх дистальнее 2 см от киля трахеи, перикард, врастании периферического узла в структуры грудной стенки, диафрагму без регионарных и отдаленных метастазов, а также при меньшем размере первичной опухоли, но с метастазами во внутрилегочных и/или корневых лимфатических узлах основным методом лечения также остается хирургический. Пятилетняя выживаемость больных составляет в среднем 50%: при ПА (T1N1M0) — 32—59% и ИВ (T2N1M0J3N0M0) — 32— 69%. У пациентов с метастазами в лимфатические узлы N1 пятилетняя выживаемость существенно варьирует в зависимости от уровня их поражения. Так, при поражении только бронхопульмональных узлов она составляет 53—64%, а указанных и корневых узлов — 30—39%. Объем операции сам по себе не влияет на отдаленные результаты, т.к. лобэктомию или пневмонэктомию выполняют по общим онкологическим принципам.
Наиболее сложной и многочисленной группой являются пациенты с местно-распространенным НМРЛ, метастазами в средостенных лимфатических узлах и/или распространением опухоли на органы и структуры средостения (ША, ШВ стадия). За последние два десятилетия расширены показания к хирургическому лечению этой сложной категории больных за счет выполнения комбинированных операций. Условно мы их подразделяем на: трахеобронхопищеводный тип (резекция бифуркации трахеи, мышечной стенки пищевода); сосудисто-пред-сердный тип (резекция перикарда, предсердия, верхней полой вены, аорты и ствола легочной артерии); парие-тально-диафрагмальный тип (резекция париетальной плевры, грудной стенки и диафрагмы). Обязательными условиями операций являются радикальность резекции смежного органа или структуры и удаление всех внутригрудных регионарных коллекторов с лимфатическими узлами средостения, т.е. расширенная медиастинальная лимфаденэктомия. Пятилетняя выживаемость больных немелкоклеточным раком легкого (T1-4N2M0, T3N1M0, T4N0M0) после комбинированного лечения в среднем составляет 18,5%, колеблясь от 13 до 30%. Широкий диапазон в результатах выживаемости больных местно-распространенным резектабельным НМРЛ Ш-А-В стадии обусловлен в первую очередь гетерогенностью группы как по символу «Т», так и особенно символу «N2» — метастатическому поражению средостенных лимфатических узлов. Неблагоприятными прогностическими факторами у этой группы больных являются: полиорганные резекции, поражение нескольких зон средостенных лимфатических узлов, локализация первичной опухоли в нижних долях, особенно с метастазами одновременно в узлах нижнего и верхнего средостения.
Послеоперационная летальность — основной показатель в оценке непосредственных результатов хирургического лечения больных раком легкого. В последние два десятилетия прогресс в хирургии привел к заметному снижению летальности, составляющей 3,2—6,2%. В МНОЙ им. П.А. Герцена послеоперационная летальность за период 1980—2005 гг. составляет 3,2%: после расширенно-комбинированной пневмонэктомии — 5,3%, пневмонэктомии — 2,7%, лобэктомии и ее вариантов — 1,9% и сублобарной резекции — 1,5%.
В плане комбинированного лечения при метастатическом поражении внутригрудных лимфатических узлов проводят лучевую терапию, полихимиотерапию или химио-лучевое лечение. Самостоятельную лучевую (химио-лучевую) терапию по радикальной программе применяют при нерезектабельном местно-рас-пространенном (ША-В стадии) немелкоклеточном раке легкого или как альтернативу хирургического лечения при функциональной неоперабельности, а также отказе пациента от операции на ранних стадиях (I—II) опухолевого процесса. По сводным данным литературы, более 5 лет после только лучевой терапии немелкокле-точного рака легкого I—II стадии переживают до 32% больных, а при местно-распространенном процессе 6—12%. Использование при лучевой терапии в качестве радиомодификатора химиопрепаратов позволяет в целом повысить отдаленные результаты при I—II стадиях до 43%. Совершенствование лучевых установок, современные методики облучения позволяют добиться лучших результатов: 91% пятилетней выживаемости при I стадии и 64% — при II стадии.
При немелкоклеточном раке легкого IV стадии возможна лишь лекарственная противоопухолевая или симптоматическая терапия.
Мелкоклеточный рак легкого (МРЛ), в отличие от немелкоклеточных форм, характеризуется ранним интенсивным лимфогенным и гематогенным метастэ-зированием и плохим прогнозом. У 80—90% больных изначально диагностируют распространенный опухолевый процесс. Поэтому многие годы мелкоклеточный рак считали «терапевтическим».
Следует отметить, что обследование больных МРЛ, его стадирование в целом не отличаются от таковых при НМРЛ. Сочетанное применение полихимиотерапии и лучевой терапии при МРЛ давно получило всеобщее признание и подтверждено многочисленными рандомизированными исследованиями. Общая 5-летняя выживаемость больных составляет 5—12%.
В последние годы при I—II стадиях, особенно неовсяноклеточном морфологическом подтипе МРЛ, признают возможность хирургического компонента в сочетании с пред- и послеоперационной полихимиотерапией. Пятилетняя выживаемость после такого лечения составляет 28—36%, лучшие (45—49%) результаты при отсутствии регионарных метастазов.

