Причина миомы матки
Современное представление о развитии миомы матки основано на гормональной теории. Нарушения экскреции и метаболического превращения эстрогенов, а также соотношения фракций эстрогенов (преобладание эстрона и эстрадиола в фолликулиновую, а эстриола — в лютеиновую фазу) приводят к морфологическим изменениям в миометрий. Масса миометрия может увеличиваться в результате как гиперплазии гладкомышеч-ных клеток, которая инициируется эстрогенами, так и гипертрофии этих клеток. Наряду с эстрогенами рост миомы стимулирует прогестерон. Гипертрофия гладкомышечных клеток при миоме матки аналогична их гипертрофии во время беременности и может возникать только при сочетанном воздействии сравнительно высоких концентраций эстрадиола и прогестерона. В лютеиновую фазу прогестерон повышает митотическую активность миомы, кроме того, прогестерон воздействует на рост миомы путем индуцирования факторов роста. В ткани миомы рецепторов эстрадиола и прогестерона больше, чем в неизмененном миометрий. Нарушение обмена половых стероидов в миоматозных узлах вызывает аутокринную стимуляцию клеток при участии так называемых факторов роста. Медиаторами действия эстрогенов в ткани миомы матки являются инсулиноподобные факторы роста I и II.
Наряду с гормональными аспектами патогенеза миомы матки немаловажную роль играют изменения иммунной реактивности организма, особенно при хронических очагах инфекции; выраженные изменения гемодинамики малого таза, а также наследственная предрасположенность. Зоны роста миомы формируются вокруг воспалительных инфильтратов и эндометриоидных очагов в миометрии. В увеличении миомы значительную роль играют фенотипическая трансформация гладких мышечных клеток и дегенеративные изменения в условиях нарушенной микроциркуляции. Зачатки миома-тозных узлов могут образовываться на эмбриональном этапе. Рост клеток-предшественников продолжается много лет на фоне выраженной активности яичников под действием эстрогенов и прогестерона.
Миомы неоднородны по структуре. По тканевому составу узлы подразделяют на миомы, фибромы, ангиомиомы и аденомиомы.
По морфогенетическим признакам выделяют 3 основные формы:
• простые миомы, развивающиеся по типу доброкачественных мышечных гиперплазии;
• пролиферирующие миомы с морфогенетическими критериями истинной доброкачественной опухоли. У каждой 4-й больной миома матки пролиферирующая с быстрым ростом миоматоз-ных узлов. Патологические митозы в пролиферирующих миомах не превышают 25%;
• предсаркомы — этап на пути истинной малигнизации. Предсаркома включает в себя множественные очаги пролиферации миогенных элементов с явлениями атипии, неоднородностью ядер клеток; количество патологических митозов достигает 75%. Однако истинная малигнизация миомы происходит менее чем в 1% клинических наблюдений.
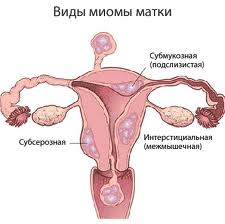
В зависимости от локализации и роста миоматозных узлов выделяют субмукозные (подслизистые) миоматозные узлы, растущие в полость матки и деформирующие ее (см. раздел «Внутриматочная патология»), и субсерозные (подбрюшинные) узлы. Миоматозные узлы растут в сторону брюшной полости. Если по мере роста мио-матозный узел расслаивает листки широкой маточной связки. Его называют интралигаментарным миоматозным узлом. Интерстици-альные (межмышечные) миоматозные узлы растут из среднего слоя миометрия и располагаются в толще миометрия.
Диагностика миомы матки
При гинекологическом осмотре отдельные субсерозные миоматозные узлы (0 тип) пальпируются отдельно от матки как округлые плотные, подвижные образования. Субсерозные узлы 1—2-го типов приводят к увеличению матки и изменению ее формы. Матка может достигать значительных размеров, ее поверхность становится бугристой, миоматозные узлы плотные, и при нарушении кровообращения их пальпация болезненна. Субсерозные узлы 3-го типа (интра-лигаментарные) определяются сбоку от матки, выполняя параметрий. Нижний полюс узла достижим при пальпации через боковой свод влагалища, узел плотной консистенции, ограниченно подвижный при попытке смещения. У больных с интерстициальной миомой пальпируется увеличенная матка плотной консистенции с гладкой или бугристой поверхностью, как правило, безболезненная.
При УЗИ субсерозные миоматозные узлы визуализируются в виде округлых или овальных образований, выходящих за наружный контур матки. Миоматозные узлы зачастую имеют слоистую структуру и так называемую псевдокапсулу, которая образуется в результате уплотнения и гипертрофии миометрия, прилежащего к миоматозному узлу. Эхогенность и звуковая проводимость зависят от гистологического
строения миоматозного узла. В однородных ги-перэхогенных миоматозных узлах преобладает фиброзная ткань. Появление интранодулярных гипоэхогенных включений указывает на некроз или кистозные полости. Гиперэхогенные включения с акустическим эффектом поглощения бывают при кальцинированных дегенеративных изменениях. Ультразвуковое сканирование позволяет обнаружить интерстициальные миоматозные узлы диаметром не более 8—10 мм. По данным УЗИ в зависимости от направления роста интерстициальных миоматозных узлов можно прогнозировать появление субмукозных и субсерозных миоматозных узлов. Центрипетальное расположение миомы указывает на рост интерстициального миоматозного узла в полость матки, при увеличении такого узла более 10 мм появляется отчетливая деформация полости матки . Центрифугаль-ный рост узлов происходит по направлению к брюшной полости . Центральный рост бывает при истинной межмышечной локализации миоматозных узлов и приводит к диффузному увеличению матки. Ультразвуковое сканирование дополняется исследованием пери- и интранодулярного кровотока для уточнения мор-фотипа опухоли. Рост миоматозных узлов зависит от увеличения кровотока в сосудистой сети матки. Плотность расположения сосудов связана с морфологическим строением и локализацией миоматозного узла. Большое количество артерий находится на периферии миоматозного узла. УЗИ, дополненное допплерографи-ей, позволяет оценить особенности кровообращения в миоматозных узлах. При простой миоме регистрируется единичный периферический кровоток, при пролиферирующей миоме — интенсивный центральный и периферический внутриопухолевый кровоток.
Для уточнения топографического расположения субсерозных миоматозных узлов можно использовать ультразвуковые томографы, дающие трехмерное ультразвуковое изображение.
Для дифференциальной диагностики субсерозных узлов и опухолей забрюшинного пространства, увеличенных лимфатических узлов, опухолей малого таза и брюшной полости наряду с УЗИ применяют компьютерную и магнитно-резонансную томографию
Диагностическая лапароскопия показана при невозможности дифференциальной диагностики между субсерозной миомой матки и опухолями брюшной полости и забрюшинного пространства неинвазивными методами.
Гистероскопия показана при появлении нарушений менструального цикла у пациенток с маткой, увеличенной не более чем на 12—13 нед беременности. При большем увеличении матки информативность гистероскопии снижается. Для исключения патологии эндометрия и слизистой оболочки цервикального канала у пациенток с метрорра-гиями и контактными кровяными выделениями независимо от величины миомы матки проводится раздельное диагностическое выскабливание слизистой оболочки матки.
Лечение миомы матки
Вопрос о целесообразности лечения при небольшой миоме матки без клинических проявлений окончательно не решен. Тем не менее таким пациенткам показано динамическое наблюдение у гинеколога с обязательным ультразвуковым контролем 1 раз в год. Больным дают рекомендации, направленные на профилактику дальнейшего роста миомы и регуляцию гипоталамо-гипофизар-но-яичниковых взаимоотношений. Из рациона исключают избыток углеводов и жиров, ограничивают острые и соленые блюда. Пациенткам рекомендуют избегать тепловых процедур, им нельзя загорать на солнце и в искусственном солярии. Миома может увеличиться вследствие массажа и физиотерапии по поводу соматических заболеваний. С целью регуляции менструальной функции рекомендуется витаминотерапия по фазам менструального цикла (фолиевая кислота и витамины группы В в первую фазу и витамины С, Е и А — во вторую фазу) или использование гормональных контрацептивов. Предпочтительны монофазные эстраген-гестаген-ные препараты и низкодозированные гестагены.
Консервативная терапия миомы матки проводится с целью торможения роста или обратного развития опухоли, лечения меномет-роррагий и анемии. С этой целью назначают производные 19-нор-стероидов (норколут, примолют-нор, норэтистерон, оргаметрил, гестринон, неместран). Под действием этих препаратов миома и, соответственно, матка уменьшаются в среднем на 1—2 нед беременности; уменьшается кровопотеря при менструации и нормализуется уровень гемоглобина. В репродуктивном возрасте гестагены назначают циклически с 16-го по 25-й день менструального цикла или с 5-го по 25-й день в течение 6—24 мес. Как правило, клинический эффект удается получить при миоме, не превышающей 8 нед беременности. У пациенток перименопаузального возраста целесообразно использовать гестагены в непрерывном режиме 6 мес, тем самым способствуя медикаментозной атрофии эндометрия и наступлению менопаузы.
Антигонадотропины, имеющие стероидную структуру (даназол, гестринон), и агонисты гонадолиберинов (золадекс, диферелин, бусерелин и др.) влияют на рост миоматозных узлов. Под действием агонистов ГнЛГ возможно уменьшение объема миоматозных узлов до 55%. Однако после прекращения приема препарата и восстановления менструальной функции у 67% больных начинается экспансивный рост миомы с признаками нарушения питания. Использование агонистов ГнЛГ целесообразно у пациенток перименопаузального периода, поскольку обусловливает стойкую редукцию стероидогенеза и наступление менопаузы. Для создания медикаментозной менопаузы применяют также антигонадот-ропины (немистран, гестринон).
Агонисты ГнЛГ используют для предоперационной подготовки к консервативной миомэктомии. Под воздействием агонистов ГнЛГ структура миоматозного узла становится более плотной, снижается интранодулярный и перинодулярный кровоток. Снижение внут-риопухолевого кровотока, а также уменьшение миомы и плотности миометрия вокруг миоматозных узлов максимально выражены после 2—3 инъекций препарата. При более длительном курсе гормональной подготовки ввиду прогрессирующей редукции артериального кровотока возможны деструктивные и некробиотические процессы в миоматозных узлах, затрудняющие консервативную миомэктомию.
Агонисты ГнЛГ могут изменить топографию интерстициально-субмукозных узлов в сторону полости матки, а интерстициально-субсерозных узлов — в сторону брюшной полости.
Использование агонистов ГнЛГ позволяет облегчить проведение лапароскопической консервативной миомэктомии и гистерэктомии у 76% больных из-за уменьшения матки и миоматозных узлов. При всех консервативных миомэктомиях после гормональной подготовки кровопотеря уменьшается на 35—40%.
С целью предотвращения менометроррагий и роста миомы применяют внутриматочную гормональную систему «Мирена», содержащую капсулу с левоноргестрелом (гестаген). «Мирену» вводят сроком на 5 лет, она обеспечивает регулярное поступление лево-норгестрела в полость матки и местное действие на эндометрий и миометрий с минимальными системными эффектами. Менструации становятся скудными, в ряде случаев наступает медикаментозная аменорея. Противопоказания для применения «Мирены»: суб-мукозные миоматозные узлы, большая полость матки, а также абсолютные показания к оперативному лечению.
Хирургическое лечение миомы матки остается ведущим, несмотря на достаточно результативные консервативные методы. Частота радикальных операций составляет 80%. Оперативные вмешательства по поводу миомы матки составляют 45% абдоминальных вмешательств в гинекологии.
Показания к хирургическому лечению больных миомой матки:
• большие размеры миомы (13—14 недель беременности);
• быстрый рост миомы (более 4 нед за год);
• субмукозное расположение узла;
• субсерозный узел 0 типа;
• нарушение питания, некроз миоматозного узла;
• шеечная миома;
• миома матки и менометроррагии, анемизирующие больную; . рост миомы в постменопаузе;
• нарушение функции соседних органов;
• бесплодие и привычное невынашивание беременности. Хирургическое лечение миомы матки может быть радикальным
или функциональным (органосохраняющим). В настоящее время имеется тенденция к снижению числа радикальных оперативных вмешательств при миоме матки и расширению показаний к органосохраняющим операциям. Функциональная хирургия матки, помимо сохранения менструальной и репродуктивной функций, позволяет предотвратить нарушение деятельности тазовых органов и способствует профилактике их опущения.
Объем оперативного вмешательства зависит от различных факторов. Хирургическое лечение миомы матки считается радикальным при выполнении гистерэктомии и включает в себя экстирпацию матки или надвлагалищную ампутацию матки без придатков. Шейка матки играет важную роль в формировании тазового дна и кровоснабжении мочеполовой системы, поэтому объем оперативного вмешательства расширяется до экстирпации матки у женщин репродуктивного возраста при рецидивирующих фоновых процессах шейки матки, лейкоплакии с дисплазией многослойного плоского эпителия, а также при шеечном и перешеечном расположении миоматозного узла. У пациенток с впервые выявленным фоновым заболеванием шейки матки следует на первом этапе проводить консервативное лечение этой патологии, а на втором — выполнять надвлагалищную ампутацию матки.
Гистерэктомию можно провести абдоминальным, лапароскопическим и вагинальным доступами. Выбор хирургического доступа зависит от величины матки, размеров и локализации миоматозных узлов, а также от опыта и квалификации хирурга.
Функциональная хирургия миомы. Существуют методы оперативного вмешательства, позволяющие сохранить адекватное кровоснабжение яичников путем выделения восходящих ветвей маточных артерий и сохранить менструальную функцию при высокой над-влагалищной ампутации, а также дефундации матки.
Менструальную и репродуктивную функции при миоме матки может сохранить консервативная миомэктомия. Миомэктомия заключается в удалении миоматозных узлов и сохранении тела матки и может осуществляться лапаротомическим, лапароскопическим и гистероскопическим доступом. Выбор хирургического доступа зависит от:
• величины матки;
. локализации миоматозных узлов;
• числа и величины миоматозных узлов;
• предоперационной гормональной подготовки;
• оснащенности эндоскопическим оборудованием;
. опыта хирурга в выполнении эндоскопических операций.
Лапаротомический доступ предпочтителен при множественных интерстициальных миоматозных узлах более 7—10 см, при низкой шеечно-перешечной локализации узлов, особенно по задней и боковой стенкам матки. Лапаротомический доступ позволяет адекватно сопоставить края ложа удаленного большого узла с наложением двурядных викриловых швов. От полноценности рубца на матке зависят течение планируемой беременности и ведение родов.
Лапароскопический доступ показан при субсерозных миоматозных узлах 0—3-го типов, а также при интерстициальных миоматозных узлах диаметром не более 4—5 см.
Отдельные субсерозные миоматозные узлы (0 тип) не представляют трудностей для эндоскопического удаления. Узел после фиксации зубчатыми щипцами отделяют от матки, коагулируя ножку, после чего пересекают ее ножницами или коагулятором. Современные мар-целяторы позволяют извлекать из брюшной полости узлы различных размеров и массы, мелкие миоматозные узлы можно извлекать через мини-лапаротомное и кольпотомное отверстия.
Интерстициально-субсерозные миоматозные узлы удаляют путем декапсуляции и энуклеации с поэтапной коагуляцией кровоточащих сосудов ложа. При значительном размере остающегося после консервативной миомэктомии ложа наряду с электрохирургической коагуляцией накладывают эндоскопические двурядные швы. Ушивание ложа узла позволяет осуществить дополнительный гемостаз, способствует профилактике спаечного процесса в малом тазу и формирует полноценный рубец.
Интралигаментарные узлы удаляют после рассечения в поперечном или косом направлении переднего листка широкой маточной связки и энуклеации.
Особую сложность представляет удаление небольших интерстициальных миоматозных узлов. Располагаясь в толще миометрия, миоматозные узлы не деформируют наружных контуров матки, что затрудняет визуальную диагностику во время операции. Показанием для удаления миоматозных узлов в этих случаях является подготовка к беременности или к стимуляции функции яичников у женщин с бесплодием. Для точной топической диагностики проводят интраоперационное УЗИ с помощью вагинального, ректального и трансабдоминального датчиков. Это позволяет точно локализовать и удалять интерстициальные узлы диаметром от I до 3 см с минимальной травмой. После ультразвуковой локализации над местом расположения узла делают небольшой глубокий разрез, миоматозный узел захватывают зубчатыми щипцами или штопором. Питающие сосуды коагулируют после энуклеации узла.
Единого мнения о числе удаляемых миоматозных узлов не существует. Тактика врача зависит от цели — сохранения репродуктивной или менструальной функции. Важно, чтобы после консервативной миомэктомии можно было пролонгировать беременность.
Эндоскопическая миомэктомия позволяет сохранить менструальную функцию у всех оперированных больных и восстановить детородную функцию у каждой 3-й пациентки. Беременность можно планировать через 6 мес после операции. После удаления больших интерстициально-субсерозных миоматозных узлов, а также после удаления интерстициальных узлов предпочтительно родо-разрешение путем кесарева сечения.
При субмукозных миоматозных узлах возможна консервативная гистероскопическая миомэктомия механическим, электрохирургическим методом и при помощи лазера (см. раздел «Внутриматочная патология»).
К консервативным хирургическим методам лечения миомы матки относят лапароскопический миолиз (вапоризация миоматозного узла при помощи лазера) и эмболизацию маточной артерии.

